
Desmistificando o Círculo de Sinner para uma limpeza inteligente
Muito se fala sobre desenvolver o melhor produto com o menor custo, mas por onde começar um desenvolvimento? Quais bases teóricas podem ser usadas para estudar um novo produto?
Este artigo vai tratar sobre um conceito muito conhecido pelos químicos: o “Círculo de Sinner” e os diferentes mecanismos de limpeza.
É importante usarmos a teoria, estruturamos nossa forma de pensar para só então partirmos para a prática.
O conceito
O conceito do Círculo de Sinner foi dado pelo alemão Herbert Sinner, chefe de tecnologia de aplicação em detergentes da empresa Henkel. Segundo ele, “a limpeza é uma operação que consiste na aplicação de um detergente a uma certa temperatura, durante o tempo necessário para dissolver ou amolecer os resíduos de modo que uma ação mecânica possa removê-los com facilidade!”
.png)
Isso significa que cada limpeza, superfície e sujeira vai precisar de diferentes combinações. É importante entender a relação entre as variáveis para chegar no melhor resultado.
Agora vamos aprofundar mais em cada fator para entender como fazer as melhores escolhas.
Ação mecânica
Este fator representa a aplicação de força física ou mecânica para a remoção de sujidades.
Existem alguns mecanismos de limpeza envolvendo a ação mecânica como é o caso da abrasão, o desgaste de um material por atrito com outro. Um exemplo na nossa rotina é quando você precisa deixar uma panela brilhando e usa uma palha de aço para tal.

Ação térmica
O aumento da temperatura aumenta a solubilidade do meio potencializando a ação dos produtos químicos e consequentemente auxiliando na limpeza. Além disso, a alta temperatura pode ser letal para muitos microrganismos, contribuindo para a desinfecção das superfícies.
O calor também desnatura as proteínas presentes em manchas orgânicas como sangue ou alimentos, facilitando a remoção na lavagem de roupas, por exemplo.
Um exemplo prático de onde o calor auxilia muito é na limpeza CIP (cleaning in place). A única ação mecânica presente neste sistema é a pressão de água que vai rodar internamente, o que nos obriga a aumentar a eficiência dos demais pontos do Círculo de Sinner, compensando este fator.
.png)
Ação do tempo
O tempo de exposição do produto químico à superfície a ser limpa influencia diretamente na eficácia. Fatores como o tipo de sujidade e a natureza da superfície interferem neste tempo, pois superfícies mais porosas demandam mais tempo de ação.
É importante se atentar à saturação da solução, pois ela reduz a capacidade de limpeza ao longo do tempo. Por este motivo é importante avaliar os fatores para determinar o melhor tempo de ação x concentração necessária.
Um bom exemplo da ação do tempo é entender como um desinfetante funciona.
A ação do desinfetante consiste em difundir-se até as células microbianas e, ao penetrá-las, desencadear reações químicas que comprometem a integridade celular, levando à morte do microrganismo. Este processo pode se dar por desnaturação de proteínas, oxidação ou até mesmo por alteração no metabolismo celular.
É possível observar, inclusive, que os rótulos de desinfetante orientam qual o tempo mínimo de contato para atingir a eficiência.
Ação química
Corresponde a ação dos produtos químicos utilizados no processo. O estudo de sinergia entre as matérias-primas usadas para constituir este produto será fundamental para o sucesso na limpeza.
Dentro da ação química, existem alguns pontos de atenção que iremos tratar abaixo.
Saponificação
A saponificação é uma reação química que ocorre entre um triglicerídeo (gordura ou óleo) e uma base forte, como o hidróxido de sódio (NaOH) ou o hidróxido de potássio (KOH). Durante essa reação, as ligações éster dos triglicerídeos são quebradas, formando moléculas de sabão (sal de ácido graxo) e glicerol.
A molécula do sabão é anfipática, com uma extremidade polar e outra apolar. Essa estrutura permite que o sabão se ligue à gordura e à água simultaneamente, formando micelas que encapsulam a sujeira e a removem.
.png)
Tensoativos:
Muitas vezes, a formulação de um produto de limpeza envolve a combinação de diferentes tipos de tensoativos para otimizar a performance. Essa sinergia pode melhorar a capacidade de remoção de sujeira, a espumação e outras propriedades desejáveis.
Os tensoativos são classificados de acordo com a natureza do grupo iônico presente em sua molécula.
.png)
Para se aprofundar mais sobre a teoria por trás dos tensoativos, clique aqui.
Emulsão
A emulsão é um dos pilares no processo de limpeza. O mecanismo parte das ligações feitas pelos tensoativos presentes nos produtos de limpeza com a sujeira na superfície a ser limpa. A emulsão faz a quebra da sujeira em pequenas partículas, formando micelas que são dispersas em líquido e, posteriormente, removidas.
Estes tensoativos chamados de emulsionantes possuem uma parte hidrófila e outra lipofílica. Essa característica permite que eles se liguem tanto às moléculas de água quanto às de óleo. Uma das formas de escolher qual tensoativo será mais adequado é usando o conceito de HLB, uma escala que indica a afinidade da substância com água ou com óleo, pois quanto maior o valor de HLB, mais hidrofílico é o surfactante. Por outro lado, quanto menor o valor de HLB, mais lipofílico ele é.
Um exemplo prático da emulsão agindo no sistema de limpeza é durante a remoção de maquiagem do rosto. Os emulsificantes se ligam às partículas de maquiagem e óleo, envolvendo-as em pequenas esferas chamadas micelas. Essas micelas são dispersas em água, tornando a maquiagem solúvel e fácil de remover. Ao enxaguar o rosto, as micelas, junto com a maquiagem e o excesso de oleosidade, são removidas da pele.

Solvência
Uma frase antiga, muito ouvida na época de escola define muito bem este mecanismo de limpeza: “semelhante dissolve semelhante”. Esta frase resume um solvente como uma substância capaz de dissolver outras, chamadas de solutos.
A capacidade deste solvente vai depender da sua natureza química, por exemplo, a água é um excelente solvente para substâncias polares, como o sal, mas não dissolve bem substâncias apolares, como a gordura.
Por sua vez, solventes orgânicos como acetona e o benzeno dissolvem bem substâncias apolares, como óleos e graxas e são utilizados em produtos de limpeza específicos, como removedores de tintas e esmaltes.

Oxirredução
Estes são processos físico-químicos complementares, oxidação e redução. Na oxidação, uma substância perde elétrons durante uma reação química, enquanto na redução, uma substância ganha elétrons durante uma reação. Elas ocorrem de forma simultânea, enquanto o agente redutor é uma substância que doa elétrons e sofre oxidação, o agente oxidante é uma substância que aceita elétrons e sofre redução.

Um bom exemplo deste processo é a ação do peróxido de hidrogênio que realiza uma ação oxidante. Ele tem a ação de branquear os tecidos, pois quando entra em contato com as moléculas dos corantes estas sofrem oxidação. Essa oxidação quebra as ligações químicas que dão cor ao tecido, fragmentando as moléculas de corante em moléculas menores e incolores.
Além de clarear o tecido, o peróxido de hidrogênio também é eficaz na remoção de manchas, como de sangue, vinho e café. Ele oxida as substâncias que causam essas manchas, tornando-as mais solúveis e facilitando sua remoção.
Decapagem
A decapagem é um processo químico que utiliza ácidos para remover impurezas e óxidos da superfície de metais. A escolha do ácido, a concentração da solução e as condições de processo são fatores cruciais para garantir a eficiência e a segurança do processo.
A decapagem ácida, a mais comum, se baseia na reação entre o ácido e os óxidos metálicos presentes na superfície. O ácido, geralmente clorídrico (HCl) ou sulfúrico (HSO), reage com os óxidos, formando sais solúveis em água e liberando hidrogênio.
Exemplo com Ácido Clorídrico e Óxido de Ferro:
Considerando o óxido de ferro (III) (FeO), uma das impurezas mais comuns em superfícies metálicas, a reação pode ser representada da seguinte forma:
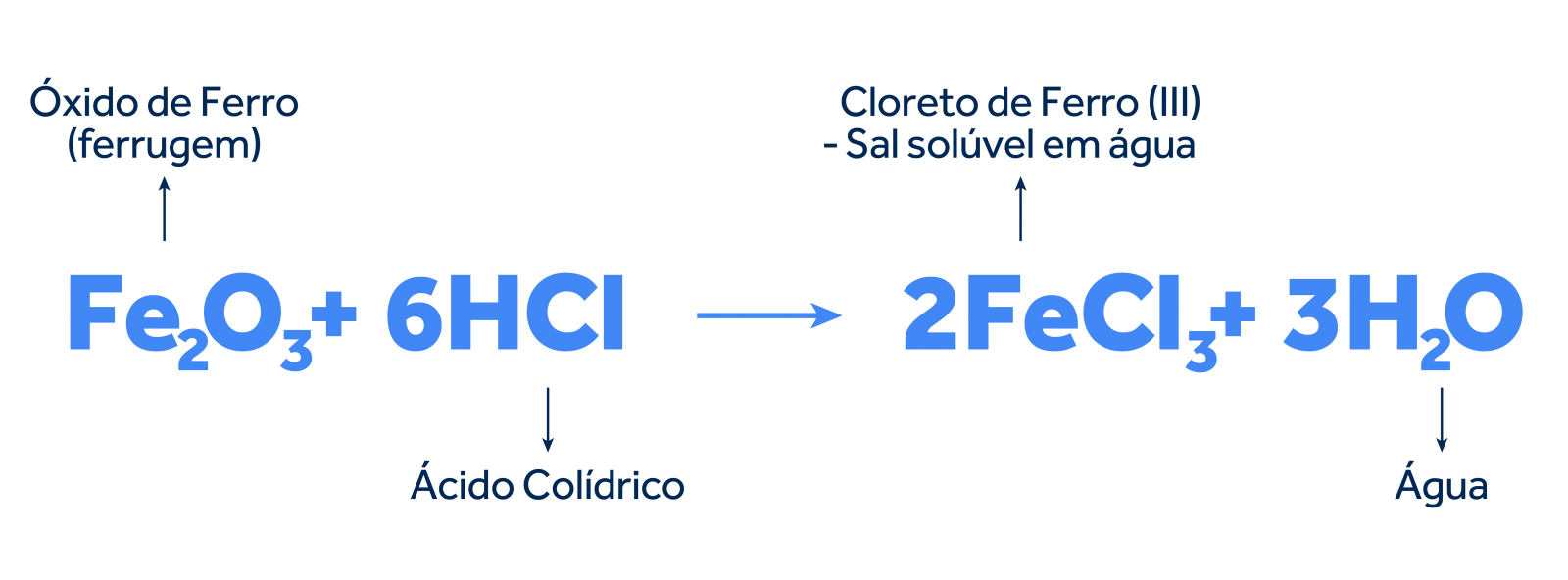
O que acontece na reação:
- Dissolução do óxido: O ácido clorídrico "ataca" a camada de óxido de ferro, quebrando as ligações químicas e formando íons de ferro e íons cloreto.
- Formação de sal: Os íons de ferro e cloreto se combinam para formar o cloreto de ferro (III), um sal solúvel em água.
- Liberação de hidrogênio: A reação também libera gás hidrogênio, que se desprende da solução.
O cloreto de ferro (III) formado na reação é solúvel em água, facilmente removido da superfície metálica por enxágue.
Os fatores que influenciam na decapagem e vão trazer um norte quanto a escolha do melhor ácido e processo vai depender do tipo de metal, espessura da camada de óxido, temperatura, agitação e demais componentes que podem influenciar nesse sistema como pintura das peças ou sujeiras de óleos e graxas.
A importância do Círculo de Sinner
Ao desmistificar o Círculo de Sinner, percebemos a complexidade da limpeza e a importância de cada etapa. Em resumo, ele nos guia para uma limpeza eficiente, mas é a personalização de cada etapa que garante o sucesso.
A Macler, com sua experiência e conhecimento técnico, oferece soluções personalizadas para cada desafio, garantindo a escolha dos produtos mais adequados e a otimização de cada etapa do processo.
Conte com a Macler como um parceiro químico e estratégico para encontrar a combinação ideal para as necessidades do seu negócio!

Leia também
Embora práticos, os amaciantes a frio tradicionais perdem em fixação de perfume e podem manchar roupas. Para resolver isso, a Macler criou uma base que une a economia desse processo à alta performance sensorial. Conheça.
Existem casos em que a espuma é indesejada, passando a ser prejudicial para o processo de limpeza. O objetivo deste artigo é elucidar os caminhos possíveis e viáveis, agilizando o processo de desenvolvimento de um produto com essa característica
Talvez um dos produtos químicos mais conhecidos e utilizados pelo consumidor brasileiro e que influencia drasticamente na cultura e comportamento no que diz respeito à limpeza é o Hipoclorito de Sódio, o famoso “cloro”.
Nossa química
Usamos nosso laboratório para criar soluções
químicas inteligentes em equilíbrio com a sua realidade.
Produtos
Usamos nosso centro de P&D, um laboratório próprio com profissionais experientes, para entregar soluções químicas inteligentes em equilíbrio com a sua realidade.
