Capacidade hidrótopa do butilglicol: comportamento na presença de álcalis e eletrólitos
O butilglicol é um composto amplamente utilizado na indústria, graças ao seu alto poder de solvência. Esse atributo também pode ser observado em soluções com álcalis em sua composição. Porém, é importante atentar-se a algumas reações inesperadas quanto à sua utilização em meios com muitos eletrólitos.
Continue a leitura para saber mais.

Butilglicol: características e aplicação
O butilglicol é um éter monobutílico de etilenoglicol. Possui características de líquido incolor com odor rançoso doce, miscível e solúvel em água e álcool, além de possuir um alto poder de solvência em hidrocarbonetos de petróleo. É composto por um glicol conectado a quatro carbonos como demonstrado na figura abaixo:
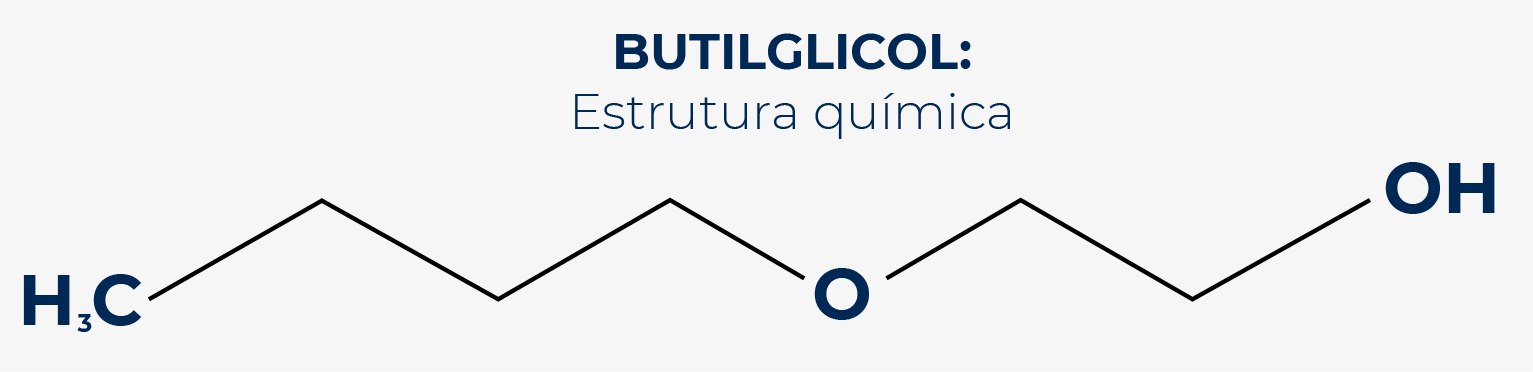
Atua na solubilização de sujidades oleosas e, principalmente, no auxílio ao tensoativo como um co-emulsionante, promovendo uma melhor molhabilidade da superfície. Além disso, glicóis de modo geral, por possuírem baixa tensão superficial, são capazes de gerar uma “película” que mascara manchas.
O butilglicol é um composto químico bastante versátil e extremamente requisitado na indústria, devido ao seu poder de desengraxe e solvência. É empregado em formulações de limpadores de modo geral, desde limpa-vidros até desengraxantes industriais e automotivos.

O que é hidrotopia?
A hidrotopia é um fenômeno de solubilização em que a adição de uma dada quantidade de um segundo soluto resulta em um aumento da solubilidade aquosa de outro soluto.
Quando é dito que o butilglicol possui um alto poder de solvência, é justamente a esse caráter de componente hidrótopo a que estamos nos referindo.
Aumento da solubilidade na presença de álcalis
Álcali é definido como qualquer hidróxido ou óxido dos metais alcalinos (lítio, sódio, potássio, rubídio e césio). Já o cáustico possui definições simples como aquele “que queima, produz cauterização, que desorganiza os tecidos cutâneos carbonizando-os”. Dessa forma, álcali cáustico é uma denominação que associa ambas as condições químicas, tendo como exemplo a famosa Soda Cáustica ou o Hidróxido de Sódio, cujo caráter corrosivo provém dessas condições.
Em produtos como desengraxantes alcalinos, por exemplo, a alcalinidade é um fator primordial para a efetividade de limpeza de sujidades como graxas, óleos e gorduras em geral. No processo de desengraxe são utilizados produtos à base de Hidróxido de Sódio e Potássio. Já a Potassa Cáustica confere maior poder de limpeza a desengraxantes.
De forma geral, o butilglicol pode ser aplicado para aumentar a solubilidade das soluções que apresentam álcalis em sua composição.
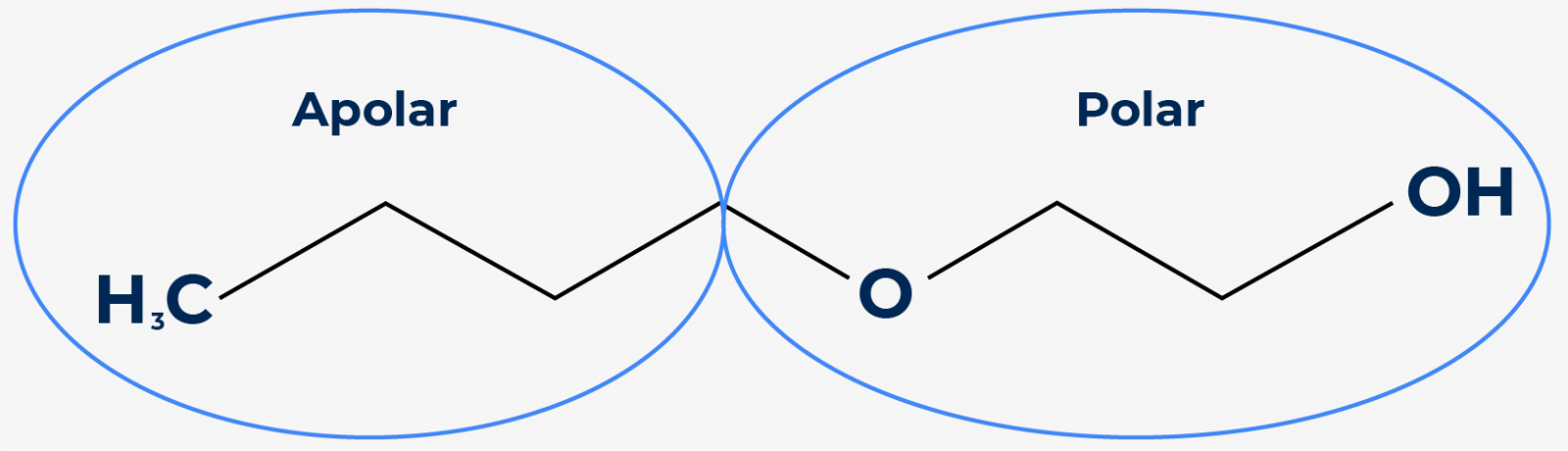
Conforme ilustrado acima, são as moléculas de oxigênio e hidroxila da parte polar que possibilitam que o butilglicol se dissolva em água. Com isso, ele criará uma mistura formando ligações de hidrogênio, diminuindo a polaridade e, consequentemente, mantendo o tensoativo mais estável.
Alta presença de eletrólitos e queda no ponto de névoa
Apesar de sua alta solubilidade na presença de álcalis, existem algumas ponderações quanto à utilização do butilglicol em meios com muito eletrólito.
Se utilizarmos um componente muito cáustico, como o Hidróxido de Sódio, e preenchermos o meio com eletrólitos, o composto não será capaz de lidar com o aumento brusco de polaridade do meio e começará a separar, rompendo as ligações de hidrogênio e água.
Isso diminuirá o ponto de névoa, que é a temperatura na qual os tensoativos, principalmente os não iônicos, tornam-se insolúveis, provocando turbidez. Caso o produto permaneça por um tempo prolongado nessa temperatura ou até acima dela, tende a ocorrer uma separação, gerando duas ou mais fases.
Pode-se afirmar então que, nesses casos, o butilglicol começará a se comportar como um óleo e, ao invés de contribuir como um agente hidrótopo, aumentando a solubilidade dos tensoativos, irá prejudicar a solubilidade do sistema como um todo.
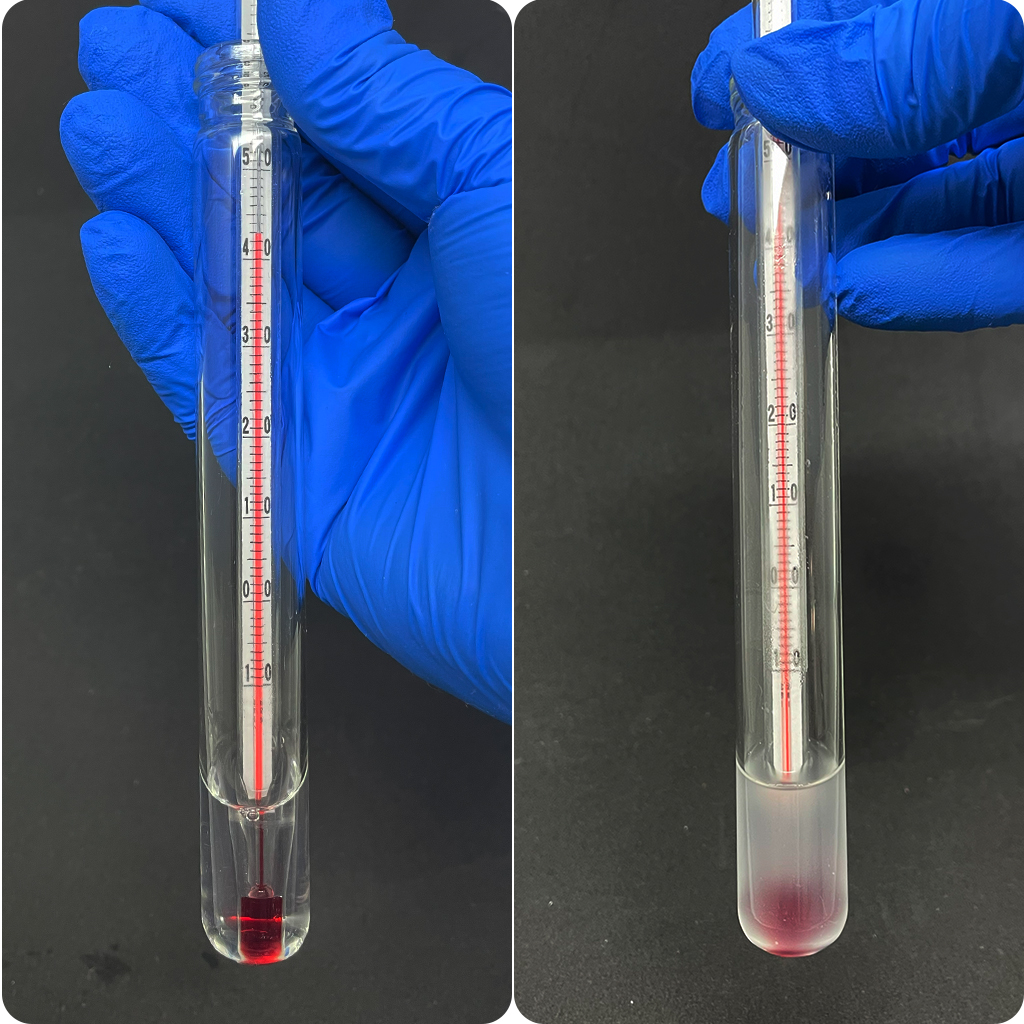
Vale destacar que quanto mais perto do ponto de névoa o produto estiver, maior será seu poder de limpeza. Dessa forma, em formulações contendo álcalis é necessário atentar-se à quantidade de butilglicol e eletrólitos dosados, de modo que se alcance um ponto de névoa de no mínimo 50°C, que é uma temperatura mínima que assegura a manutenção da integridade do produto durante a estocagem e transporte.
Em alguns produtos mais técnicos específicos, onde se conhece a temperatura de aplicação no momento do consumo, formular o produto de forma que o ponto névoa fique levemente abaixo da temperatura de aplicação contribui para a máxima eficiência de limpeza.
Opções para substituir o butilglicol na presença de eletrólitos
Conforme vimos acima, a utilização do butilglicol em meios com muitos eletrólitos pode diminuir o ponto de névoa e prejudicar a solubilidade da formulação como um todo.
Nesse sentido, a Macler possui hidrótopos de altíssima eficiência que garantem excelentes resultados com baixas dosagens. Confira abaixo um exemplo de alguns deles aplicados em um desengraxante industrial cáustico.

Clique aqui e conheça algumas soluções de Macler para substituir o butilglicol nas suas formulações.
Leia também
Embora práticos, os amaciantes a frio tradicionais perdem em fixação de perfume e podem manchar roupas. Para resolver isso, a Macler criou uma base que une a economia desse processo à alta performance sensorial. Conheça.
Existem casos em que a espuma é indesejada, passando a ser prejudicial para o processo de limpeza. O objetivo deste artigo é elucidar os caminhos possíveis e viáveis, agilizando o processo de desenvolvimento de um produto com essa característica
Talvez um dos produtos químicos mais conhecidos e utilizados pelo consumidor brasileiro e que influencia drasticamente na cultura e comportamento no que diz respeito à limpeza é o Hipoclorito de Sódio, o famoso “cloro”.
Nossa química
Usamos nosso laboratório para criar soluções
químicas inteligentes em equilíbrio com a sua realidade.
Produtos
Usamos nosso centro de P&D, um laboratório próprio com profissionais experientes, para entregar soluções químicas inteligentes em equilíbrio com a sua realidade.